Trouxemos essa matéria para, mais uma vez, mostrar a todos a importância do controle de qualidade para a SEGURANÇA DO PACIENTE, em cada processo, material e atendimento.
Falhas na comunicação de fornecimento e produção irregular de medicamentos motivaram as multas / Foto: Freepik
 Agência endurece discurso regulatório ao negar todos os recursos da indústria contra penalidades em 2025
Agência endurece discurso regulatório ao negar todos os recursos da indústria contra penalidades em 2025
por Leandro Luize em 26/01/26 às 10:45 e atualizado em 26/01/26 às 11:01
Multas para farmacêuticas somam R$ 4,6 milhões
FATO: A Anvisa negou todos os recursos apresentados por grandes indústrias farmacêuticas contra multas aplicadas em 2025, mantendo ao menos R$ 4,6 milhões em penalidades. A decisão envolveu os principais grupos do setor e reforçou a leitura mais restritiva da agência sobre falhas regulatórias
IMPACTO: A postura da autarquia eleva o grau de atenção dos laboratórios sobre compliance regulatório, rastreabilidade e comunicação com o regulador. O movimento também aumenta a previsibilidade do enforcement, ao deixar claro que porte, histórico ou capacidade técnica não mitigam infrações formais
PERSPECTIVA: A linha dura adotada em 2025 tende a se consolidar em 2026, alinhada à agenda regulatória da Anvisa. Para a indústria, o desafio será equilibrar rigor sanitário, eficiência operacional e diálogo institucional
 A Anvisa encerrou 2025 reforçando uma postura de rigor regulatório frente às maiores indústrias farmacêuticas do país. Ao longo do ano, a Diretoria Colegiada negou todos os recursos apresentados por grandes laboratórios contra multas aplicadas em processos de fiscalização, mantendo ao menos R$ 4,6 milhões em penalidades.
A Anvisa encerrou 2025 reforçando uma postura de rigor regulatório frente às maiores indústrias farmacêuticas do país. Ao longo do ano, a Diretoria Colegiada negou todos os recursos apresentados por grandes laboratórios contra multas aplicadas em processos de fiscalização, mantendo ao menos R$ 4,6 milhões em penalidades.
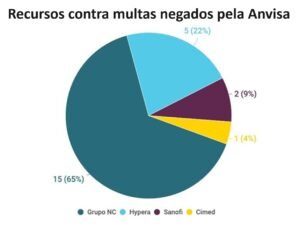
O dado tem como base as decisões publicadas pela agências envolvendo os cinco maiores grupos farmacêuticos nacionais. O Grupo NC, controlador da EMS, Germed, Legrand Pharma e Multilab, concentrou o maior número de recursos (15). Na sequência aparecem Hypera (5), Sanofi (2) e Cimed (1).
O resultado chama atenção não apenas pelo volume financeiro, mas pelo fato de nenhum recurso ter sido acolhido, sinalizando uma leitura mais restritiva da agência sobre falhas regulatórias, especialmente aquelas ligadas a deveres formais de informação, autorização prévia e cumprimento de ritos administrativos.
Remédio para autismo integra lista de penalidades
Entre os julgamentos mais sensíveis está a manutenção de uma multa de R$ 150 mil aplicada à EMS. O motivo é que a farmacêutica brasileira não comunicou à Anvisa uma queda de 56% no fornecimento de risperidona, em 2012. O medicamento é utilizado no tratamento de sintomas de autismo e integra terapias de uso contínuo, com impacto direto sobre pacientes e sistemas de saúde.
Ao votar pela manutenção da penalidade, o diretor-relator Thiago Lopes foi categórico ao afirmar que a infração se configura independentemente da ocorrência de dano concreto. “A omissão do dever de informar, por si só, já frustra a política de vigilância sanitária e consuma o ilícito”, declara.
Em outro processo, a Diretoria Colegiada confirmou multa para a EMS por ter produzido 154 medicamentos em uma fábrica que ainda não havia recebido autorização formal de funcionamento. O fato ocorreu em 2015.
O discurso das indústrias: correção imediata e segurança do paciente
Em posicionamento oficial, o Grupo NC defendeu a legitimidade do uso de recursos administrativos e buscou afastar qualquer interpretação de negligência regulatória. Segundo a empresa, a interposição de recursos não representa reconhecimento de irregularidades e não posterga a adoção de medidas corretivas.
“A apresentação de recursos administrativos contra autos de infração e multas é um instrumento legítimo de defesa, previsto na legislação brasileira, utilizado de forma técnica e dentro das regras do processo regulatório”, reiterou o grupo em nota oficial.
A empresa ressaltou ainda que eventuais não conformidades são tratadas de forma imediata, independentemente da tramitação administrativa. “Essas penalidades possuem natureza eminentemente administrativa e costumam ser formalizadas em momento posterior à regularização já efetuada, não havendo qualquer prática de aguardar o desfecho da discussão administrativa para resolver questões operacionais, regulatórias ou de segurança”, complementa o comunicado.
No caso específico da produção em fábrica sem aval formal, a EMS declarou que os medicamentos citados estão “plenamente regulares e seguros para a população”.
A Sanofi também adotou um tom institucional e reafirmou compromisso com as normas regulatórias. “Eventuais recursos apresentados à Anvisa ocorrem no âmbito regular dos processos administrativos, conforme previsto na legislação brasileira. A companhia reafirma seu compromisso com o cumprimento das normas regulatórias, com a ética, com a qualidade e a segurança de seus produtos”, informou a empresa.
Hypera e Cimed foram procurados pela reportagem, mas não responderam aos questionamentos.
Entidades setoriais: apoio à vigilância, alerta para previsibilidade
Embora não tenham comentado diretamente os autos específicos julgados pela Anvisa, entidades da indústria farmacêutica realçaram a necessidade de equilíbrio entre rigor sanitário e previsibilidade.
“A atuação da Anvisa é fundamental para garantir a segurança dos pacientes. Para a indústria, é igualmente essencial que o ambiente regulatório ofereça previsibilidade, segurança jurídica e diálogo técnico contínuo, permitindo planejamento de longo prazo, investimentos e inovação”, comenta Nelson Mussolini, presidente executivo do Sindusfarma.
“Uma autarquia técnica, estruturada e previsível é um ativo do país. O desafio é fortalecer a capacidade regulatória com foco preventivo e eficiência, evitando assimetrias e gargalos que impactem o abastecimento e a competitividade da indústria brasileira”, observa Reginaldo Arcuri, presidente do Grupo FarmaBrasil.
Comportamento em linha com agenda regulatória de 2026
A postura da Anvisa acompanha a agenda regulatória prevista pela agência para 2026. O documento funciona como um mapa estratégico e reúne 161 temas prioritários a serem regulamentados ao longo do ano.
Entre as novidades está prevista uma ampliação considerável no uso de ferramentas de inteligência artificial. “A ideia é implementar recursos que agilizem processos internos e acelerem a publicação de normas, o que tende a aumentar o patamar de exigência na produção de medicamentos pela indústria”, reforça Michelle Reis, consultora da área regulatória e uma das integrantes da seção Os Especialistas do Panorama Farmacêutico.
O objetivo é reduzir os gargalos presentes da agência, que crescem ano a ano com o acúmulo de pendências gerado pelo aumento da demanda somado à diminuição da equipe da autarquia, que contava com 2.366 servidores em 2007 e finalizou o ano passado com 1.514. Com o Concurso Nacional Unificado e a expectativa de chamadas adicionais, a meta é atingir aproximadamente 1.620 servidores ainda em 2026.
fonte: Panorama Farmacêutico
material enviado pela Dra. Célia Wada – farmacêutica – CRF SP 7043 / CRF RJ 34658

